
Impulse by ICO lance AIforHer, un challenge inédit entre startups et personnel médical qui associe l’intelligence artificielle à l’humain pour accélérer la lutte contre le cancer du sein

Le cancer du sein se traite de mieux en mieux mais cela ne suffit pas : il faut davantage diagnostiquer et mieux cibler les traitements. Avec l’arrivée de nouvelles thérapies ciblées pour les patientes présentant une faible ou très faible expression du récepteur HER2, un impératif clinique s’impose : affiner et fiabiliser le diagnostic de ce biomarqueur devenu central dans les décisions thérapeutiques.
Cette exigence de précision entre en résonance avec un autre bouleversement : l’essor de la pathologie digitale et des algorithmes d’intelligence artificielle capables d’assister les pathologistes dans l’évaluation fine du HER2. Si ces technologies sont prometteuses, leur déploiement en routine clinique pose encore des questions cruciales : fiabilité, robustesse, interprétabilité et acceptabilité par les professionnels.
C’est à cette jonction, entre progrès thérapeutique et innovation technologique qu’émerge un besoin terrain fort : garantir que les outils d’IA désormais disponibles répondent aux exigences cliniques et s’intègrent efficacement dans les pratiques médicales.
Pour relever ce défi, plusieurs acteurs se mobilisent, forts de leur complémentarité et de leur engagement commun en faveur de l’innovation au service des patients :
Ensemble, ces partenaires lancent AI for Her, un appel à solutions pour identifier, tester et faire émerger les meilleures technologies d’IA appliquées à la pathologie digitale dans le cancer du sein.
L’objectif est clair : permettre à chaque patiente de bénéficier d’une thérapie la plus adaptée, le plus tôt possible.

AI for Her
Les pionniers des plus grandes découvertes et avancées scientifiques ne se sont pas lancés seuls. La compétition positive, l’esprit d’équipe, l’ambition collective au service d’un meilleur demain, ont été des moteurs extraordinaires de développement.
AI for Her se veut être un challenge inédit et un mouvement collectif de coopétition alliant le monde technologique et scientifique pour améliorer la prise en charge et le traitement des patientes atteintes du cancer du sein et aider le personnel médical en apportant toujours plus de précision, d’objectivité et de reproductibilité à leurs diagnostics.
Pendant 6 à 9 mois, anatomopathologistes et startups portant une solution d’intelligence artificielle capable de réaliser un scoring HER2 (une des typologies du Human Epidermal growth factor Receptor, ou récepteurs de facteur de croissance épidermique humain jouant un rôle clé dans le cancer du sein) à faible et ultra faible expression, vont croiser leurs expertises et concentrer leurs énergies à l’évaluation des performances et de l’usage des algorithmes d’IA.
AI for Her est le tout premier challenge à permettre l’évaluation d’algorithmes d’IA en vie réelle, au coeur de l’hôpital, grâce à l’organisation de tout un centre de lutte contre le cancer.

*Le lancement des études A et B est conditionné à la contractualisation avec l’ensemble des parties prenantes.
Pour l’étude A, la temporalité indiquée est celle de l’étude complète intégrant l’analyse statistique des résultats. La durée de scoring des algorithmes est à déterminer mais s’étalera sur un délai plus court (de quelques jours)
Pour l’étude B, la temporalité indiquée concerne les trois étapes de scoring (sans IA, avec IA A, avec IA B) qui s’étaleront chacune sur quelques jours ainsi qu’un mois de “wash-out” prévu entre chaque étape pour assurer l’objectivité de résultat. La temporalité peut s’étendre jusque fin février en comptant l’analyse des résultats finaux.

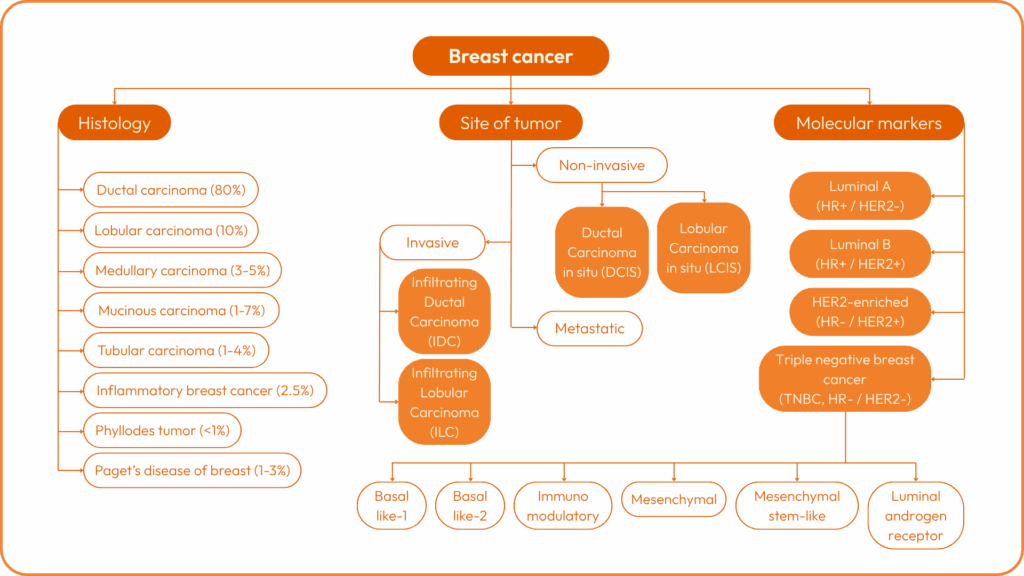
Il existe plusieurs types de cancer du sein :
Chaque cancer est ensuite caractérisé par un stade de I à IV, et par un grade de I à III. Le stade 4 représentant un cancer métastatique.
On peut ensuite déterminer des sous-types de cancer selon l’expression (ou non) de certains biomarqueurs moléculaires :


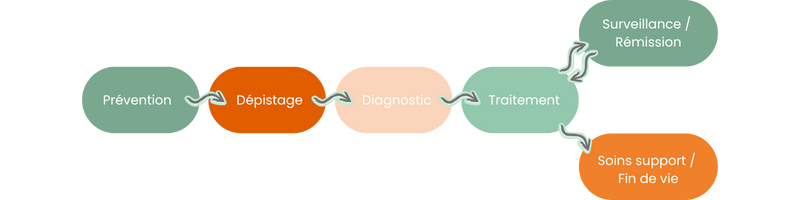
La phase de dépistage est majoritairement réalisée en médecine de ville, par mammographie.
Au cours de la phase de diagnostic, plusieurs consultations sont réalisées :
L’annonce du diagnostic se fait le jour-J ou sous une semaine si la biopsie a du être faite lors de cette consultation initiale.
C’est à partir de la biopsie que débute le travail du laboratoire d’anatomopathologie, qui va alors :
Le choix de la coloration dépend du diagnostic recherché ; Par exemple, la coloration HES (Hématoxyline – Éosine – Safran) permet plutôt un diagnostic standard, là où la coloration IHC (Immunohistochimie) permet d’identifier des protéines ou antigènes cibles et donc des sous-type de cancer.
Dans notre challenge, nous travaillons sur des lames IHC.
La coloration se fait ensuite avec un couple automate / anticorps. Le choix de l’anticorps va dépendre de la cible.
Dans le cadre du HER2, il faut :
Morgane MENARD
Responsable de l’Accélérateur IMPULSE by ICO
morgane.menard@ico.unicancer.fr
Antoine GUYONVARCH
Chef de projet innovation et santé numérique
antoine.guyonvarch@ico.unicancer.fr
